14
2022-07
膀胱癌是全球第九大常见癌症[1]。临床上约有75%的膀胱癌患者为非肌层浸润性膀胱癌(NMIBC)[2],其余为肌层浸润性膀胱癌(MIBC),NMIBC患者通常在经尿道电切术后进行膀胱内治疗,然而大约60%的患者会在治疗后2年内复发,且25%患者会进展到晚期。MIBC常发生转移性扩散是患者低生存率的主要原因[3]。值得庆幸的是,近年来膀胱癌免疫治疗取得了巨大的进步,各种免疫疗法,包括BCG(卡介苗)膀胱灌注和免疫检查点阻断疗法,在早期和晚期膀胱癌患者中获得持久的临床获益。膀胱癌类器官为检测免疫治疗反应提供了一个合适的实验肿瘤模型,这可以转化为其他实体癌症的治疗方法。其中嵌合抗原受体(CAR)-T细胞是一种很有前景的实体癌个体化免疫治疗工具[4]。
CAR-T疗法
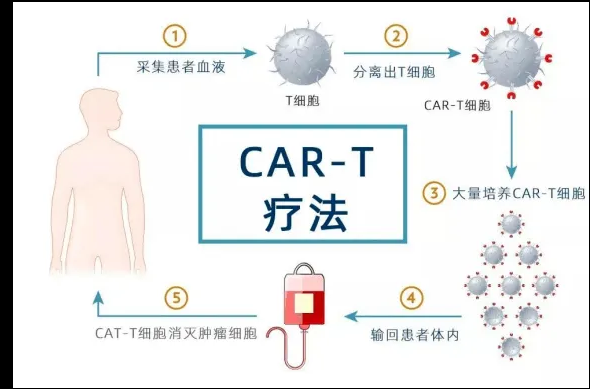
CAR-T疗法就是嵌合抗原受体T细胞免疫疗法,是一种很有前途的针对实体癌症的个性化免疫治疗工具,因为它们可以修饰成针对任何肿瘤相关抗原(TAA)的CAR,其原理是通过基因工程技术,将T细胞激活,并装上定位导航装置CAR(肿瘤嵌合抗原受体),将普通的T细胞武装成具有“定向导航”的超级战士,专门识别并高效灭杀肿瘤细胞,从而达到治疗恶性肿瘤的效果。这是一种治疗肿瘤的新型精准靶向疗法,近几年通过优化改良在临床肿瘤治疗上取得很好的效果。
研究
背景
任何旨在取得临床成功的个性化免疫治疗策略都必须通过大量临床前实验进行评估和验证。目前,细胞系和患者衍生异种移植物动物模型(PDX)是临床前评估的最常见选择[5]。然而,细胞系相对缺乏肿瘤特性,尽管它易于体外扩增,却不利于评价治疗效果。而PDX模型虽然允许体内筛选,在建模方面却需要耗费大量时间和资源。
虽然多项CAR-T细胞治疗膀胱癌的临床试验项目陆续登记并开展,但目前尚未有任何实验室研究结果或数据被公布。在这个阶段,开发一种针对膀胱癌的个性化CAR-T细胞免疫疗法势在必行。因此,有必要构建合适的模型来研究CAR-T细胞对膀胱癌的疗效。

本篇小编就带大家一起解读这篇来自期刊Clinical & Translational Immunolog的论文 Patient-derived organoids of bladder cancer recapitulate antigen expression profifiles and serve as a personal evaluation model for CAR-T cells in vitro (膀胱癌类器官再现来源肿瘤表面抗原表达谱特征可以作为CAR-T细胞体外个体化评价模型),本文旨在一起探讨以患者来源肿瘤类器官实验评价CAR-T细胞免疫疗法在膀胱癌中的效用,实验研究团队希望建立一个肿瘤类器官体外技术平台来评估CAR-T细胞介导的抗膀胱癌细胞毒性。
研究
思路
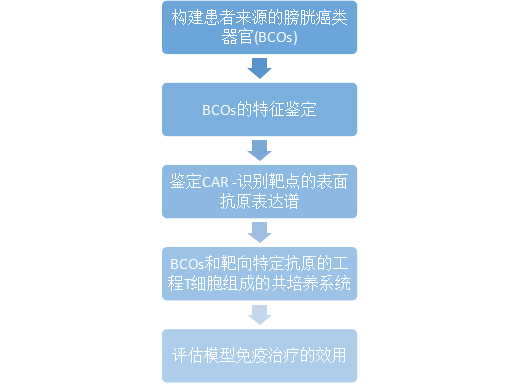
研究
结果
01
⚪在组织学特征上验证了膀胱癌类器官高度还原亲代肿瘤
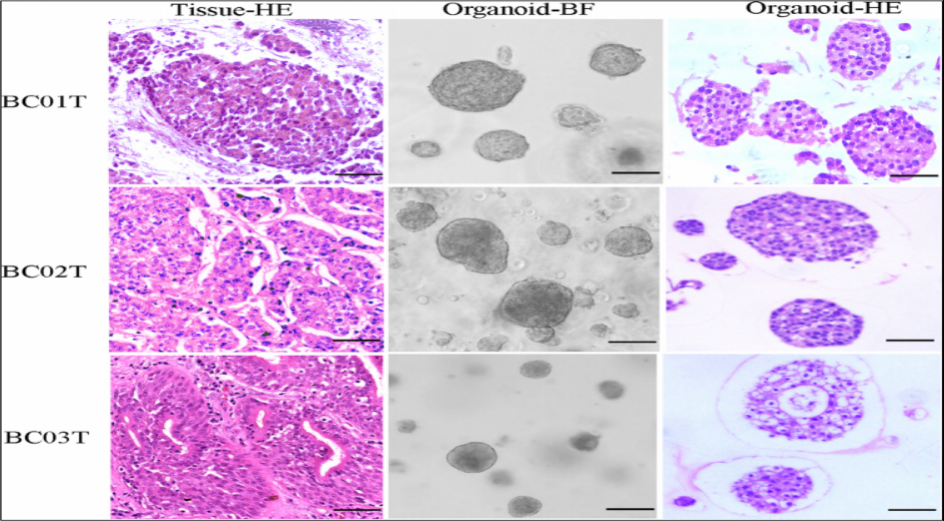
★
PIC.01
02
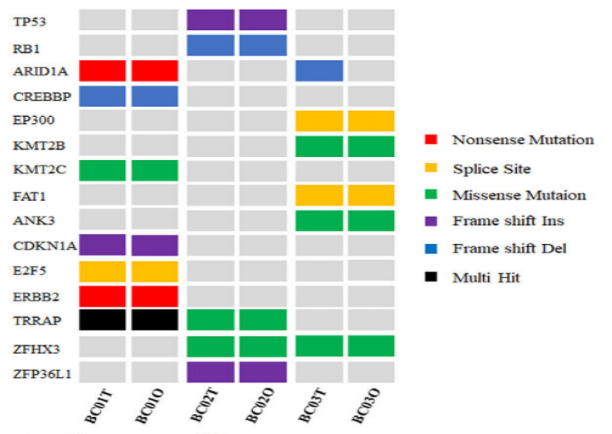
⚪在基因突变谱上验证了膀胱癌类器官细胞系高度保留亲代肿瘤特征
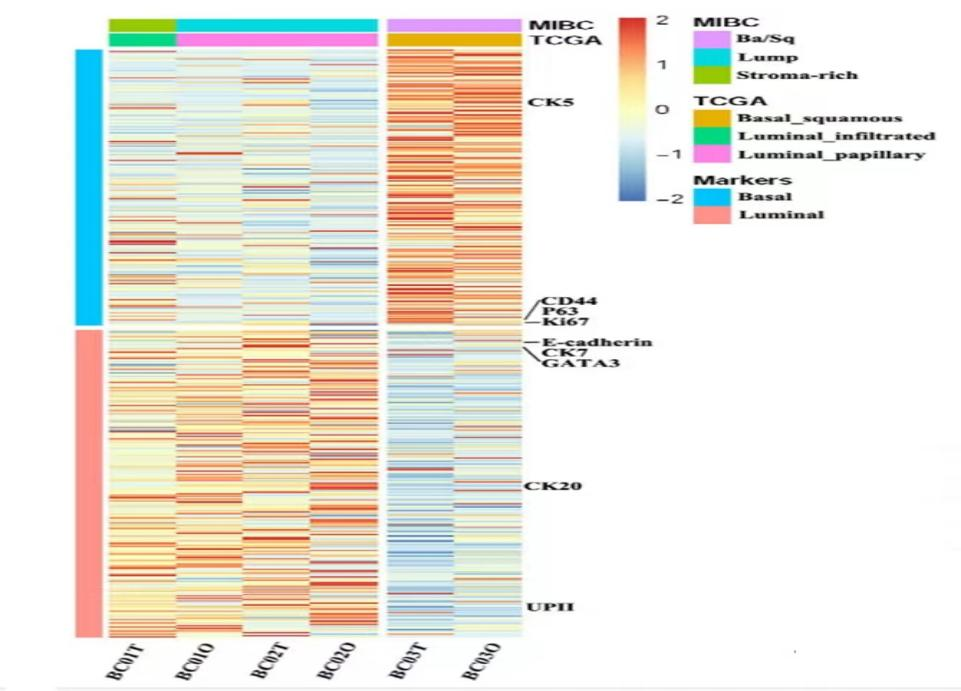
★
PIC.02
(注:膀胱癌类器官及其原发肿瘤的基因表达和基因突变图谱显示BCOs的基因表达谱与原发肿瘤组织的基因表达谱高度相似)
 |  |
 | |
★
PIC.03
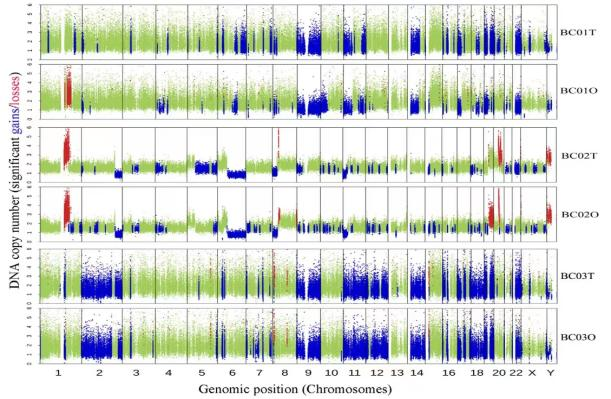
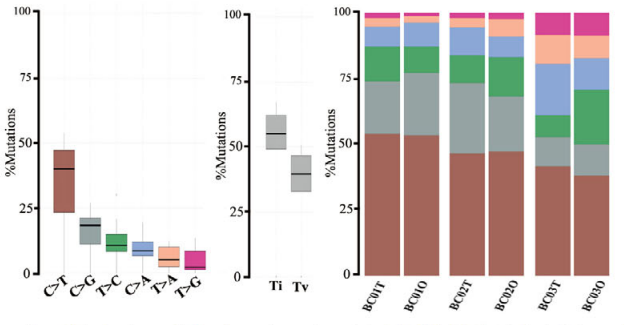
(对肿瘤及其来源的BCOs的WES分析BCOs高度重现了其来源的原发性肿瘤的基因组图谱)
03
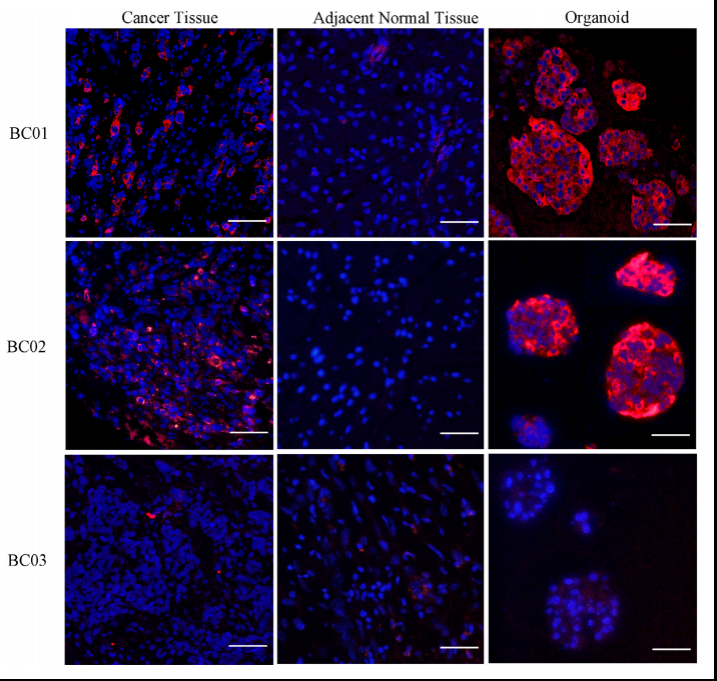
⚪MUC1在膀胱癌类器官及其原发肿瘤中一致高表达
★
PIC.04
(注:免疫荧光分析显示MUC1在相应的BCO中持续表达,但在癌旁的正常组织中不表达。因此,本实验选择MUC1作为CAR-T疗法的靶标)
04
⚪成功构建了MUC1特异性CAR-T细胞
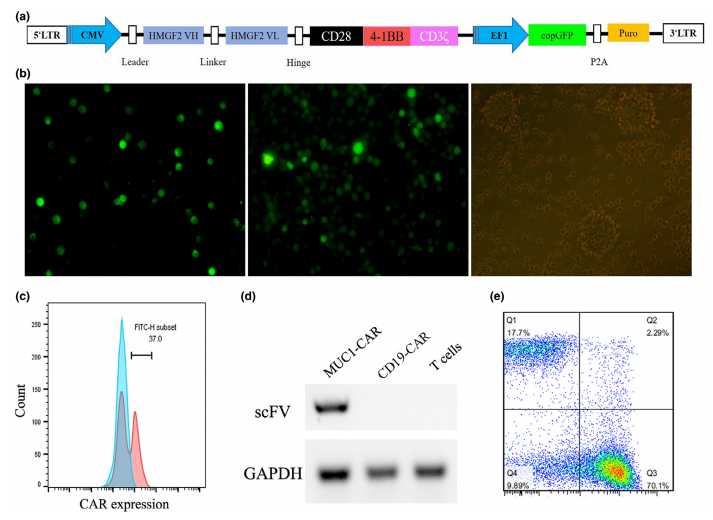
★
PIC.05
(流式细胞仪分析在转导7天后,CD4+:CD8+T细胞的比率约为1:3,观察到CAR-T细胞和CD19 CAR-T细胞之间没有显著差异)
05
⚪成功激活CAR-T细胞的特异性抗原识别和免疫
为了评估构建的BCOs在膀胱癌免疫治疗反应方面中的效用,研究人员将MUC1+BCO与MUC1靶向CAR-T细胞进行共同培养。
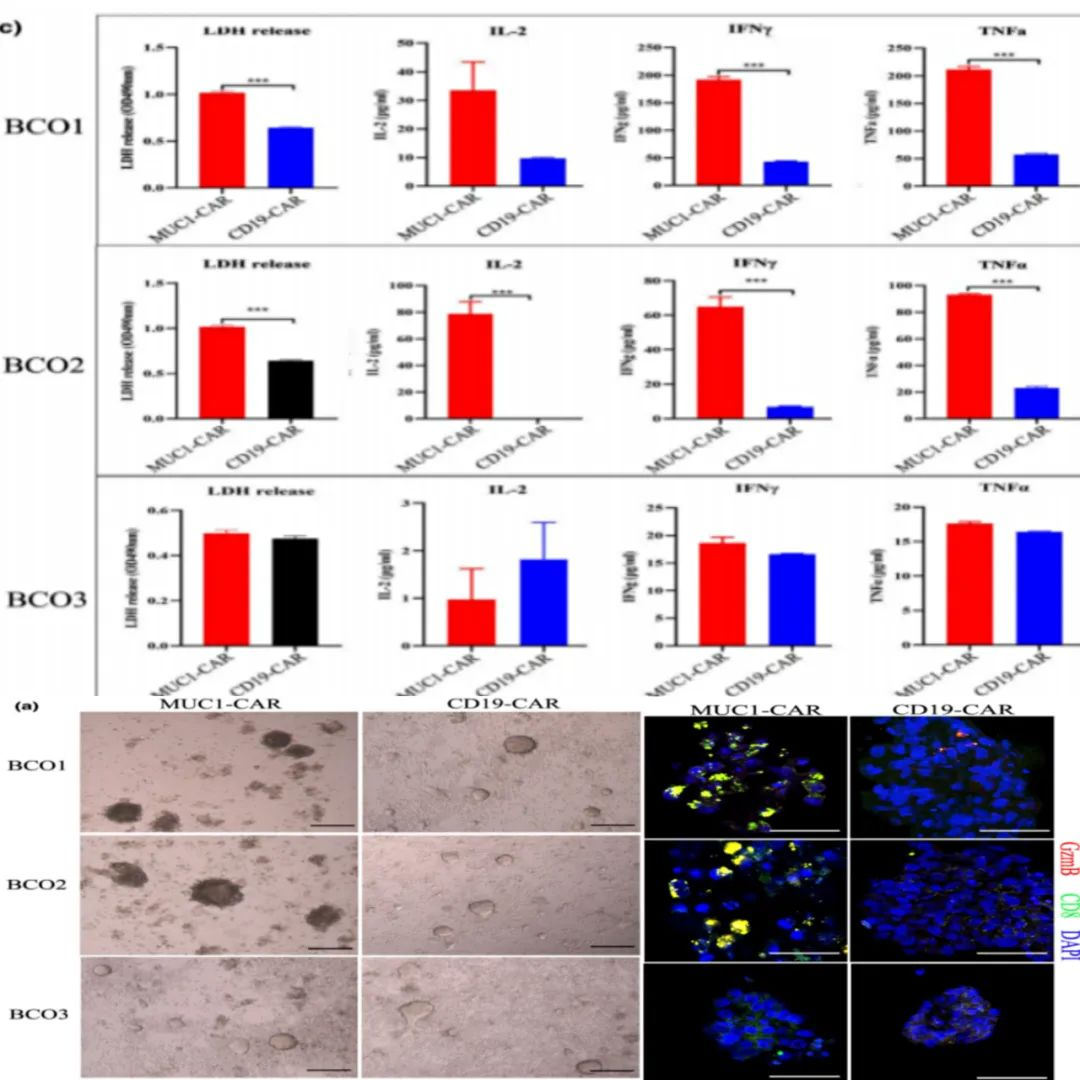
★
PIC.06
研究结论
患者来源的BCO再现了亲代膀胱癌组织的异质性和关键特征,该实验中构建的BCO正是合适的研究CAR-T细胞介导的膀胱癌治疗的模型。构建患者来源的膀胱癌类器官可以用于体外CAR-T细胞的临床前测试。
小结
综上所述,患者来源细胞构建的肿瘤类器官模型在试验中的表现与亲缘细胞高度相关,具有作为体外临床前测试模型广泛推广的价值。事实上,类器官技术由2009年类器官技术元年发展至今,研究应用潜力变得逐渐清晰。如今,不论是疾病机制研究、新药研发、临床药敏测试、药物高通量筛选等领域都能看到类器官的活跃身影。随着类器官技术的不断推广和更广泛的应用,其高效、准确、快速等优势也将在科研、临床等领域展现出更加广阔的前景!
精科医学
精科医学作为国内类器官技术转化先行者,对膀胱癌类器官的相关研究与临床应用更是走在行业前列。我们在膀胱癌类器官培养上积累了丰富经验,精科类器官团队利用成熟的样本处理技术和培养基配方,对经尿道膀胱肿瘤电切术及根治性膀胱切除术取得肿瘤样本进行处理,临床建模成功率较高,且大多能稳定传代培养,甚至可传代至第6代以上仍然保持较高增殖能力。此外,我们还和多家医院和科研机构开展科研和临床合作。目前我们已经在类器官建模方法、类器官鉴定、药物敏感性检测方法、类器官共培养等多个重要方法学上实现突破,并已建立相关实验室标准。
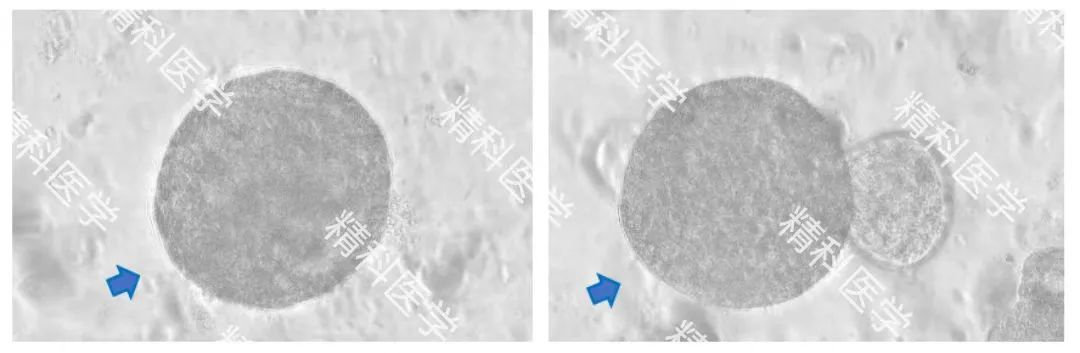
★
PIC.07
某患者膀胱癌类器官培养案例(图片来源:精科类器官平台实验室)
·参考文献:
[1]Antoni S, Ferlay J, Soerjomataram I, Znaor A, Jemal A, Bray F. Bladder cancer incidence and mortality: a global overview and recent trends. Eur Urol 2017; 71: 96–108.
[2]Kamat AM, Hahn NM, Efstathiou JA et al. Bladder cancer. Lancet 2016; 388: 2796–2810.
[3]Martinez VG, Munera-Maravilla E, Bernardini A et al. Epigenetics of bladder cancer: where biomarkers and therapeutic targets meet. Front Genet 2019; 10: 1–24.
[4]Koneru M, Purdon TJ, Spriggs D, Koneru S, Brentjens RJ. IL-12 secreting tumor-targeted chimeric antigen receptor T cells eradicate ovarian tumors in vivo. Oncoimmunology 2015; 4: e994446.
[5]Jarno Drost HC. Organoids in cancer research. Nat Rev 2018; 18: 407–418.