15
2022-09
Citation引文
肝细胞癌(HCC)是世界上最常见的原发性肝癌,也是癌症相关死亡的第二常见原因。肝细胞肝癌是肝脏最常见的恶性肿瘤,恶性程度高,容易出现复发和转移。多激酶抑制剂索拉非尼是晚期肝癌的唯一治疗选择。由于肿瘤的异质性,其疗效因患者而异,并且由于不良反应和耐药性而受到限制。
临床前药物开发的一个主要障碍是缺乏合适的细胞培养模型系统。目前常用的人类癌症模型包括癌细胞系和患者来源的异种肿瘤移植的动物模型,尽管这两类模型为癌症的研究作出了重要贡献,但仍有一些局限性。癌细胞系可能已经发生了重大的遗传变化,无法再现原始肿瘤的遗传异质性;而动物模型对患者肿瘤亚群的植入效率有限,且模型生成耗时、造价昂贵,甚至可能经历动物特异性肿瘤进化而不能真实有效地模拟患者的致病过程。因而兼具较好还原原代肿瘤特征并消耗较少的建模时间的患者来源类器官成为了科研临床的新选择。
今天,小编给大家带来Cell Reports 的一篇文章,了解患者来源的类器官如何代表患者“替身试药”从而助力临床肝癌个体化新疗法开发。在该研究中,团队选择运用患者活检组织构建HCC类器官进行索拉非尼药物敏感度测试,用以研究肿瘤异质性导致的个体药效差异。
首先,团队利用HCC患者的穿刺活检组织成功构建HCC类器官,并成功验证了类器官与亲代肿瘤的一致性。再使用肝内胆管癌(CCC)患者的组织构建CCC类器官,发现其与亲代组织同样具有较高的一致性。最后,团队使用HCC类器官和CCC类器官对索拉非尼进行药敏试验,发现不同患者来源的类器官对索拉非尼具有不同的敏感性。该研究证明,由患者活检组织来源的类器官模型与亲代肿瘤组织高度一致,能为开发个体化精准治疗提供工具。
研究结论
一
穿刺活检组织构建患者来源HCC类器官和正常肝组织类器官
在超声引导下从HCC患者中获得肿瘤和正常肝组织穿刺活检样本,最终从8名患者中建立10个HCC类器官系进行分析。

图1 肝癌患者来源肿瘤类器官/正常肝组织类器官建模
图2 患者肿瘤和正常肝组织穿刺活检组织
1
HCC类器官再现亲代肿瘤组织
病理学特征
对肿瘤类器官及其活检组织石蜡包埋切片进行组织学分析和评估,结果显示HCC类器官维持了原发HCC的生长模式和分化级别(图3)。
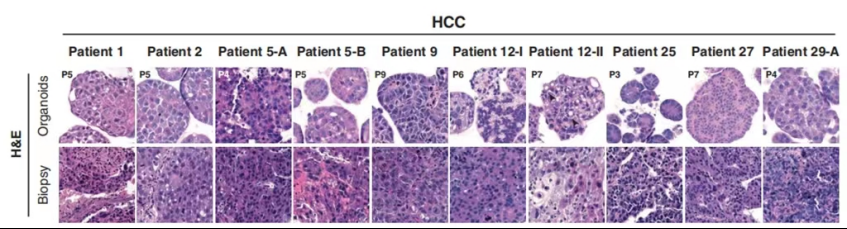
图3 HCC类器官及其活检组织HE染色图
2
HCC类器官保留亲代肿瘤的
体细胞基因突变
对7个HCC类器官以及亲代肿瘤活检样本以及成对的正常肝活检组织进行了全外显子测序(WES)。结果显示,类器官的体细胞突变数量与对应的肿瘤活检的突变数量没有显著差异。
3
患者来源肝癌类器官注射到免疫缺陷
小鼠体内会成瘤且还原亲代肿瘤特征
将所得HCC类器官皮下注射到免疫缺陷小鼠体内,发现所有成功移植的类器官(HCC类器官和CCC类器官)均产生异种移植瘤,且再现了类器官和原代肿瘤的组织学特征和肿瘤标记物表达(图4)。相对的,对应的正常肝类器官并未产生肿瘤,证明了患者来源肝癌类器官具有小鼠体内成瘤能力。
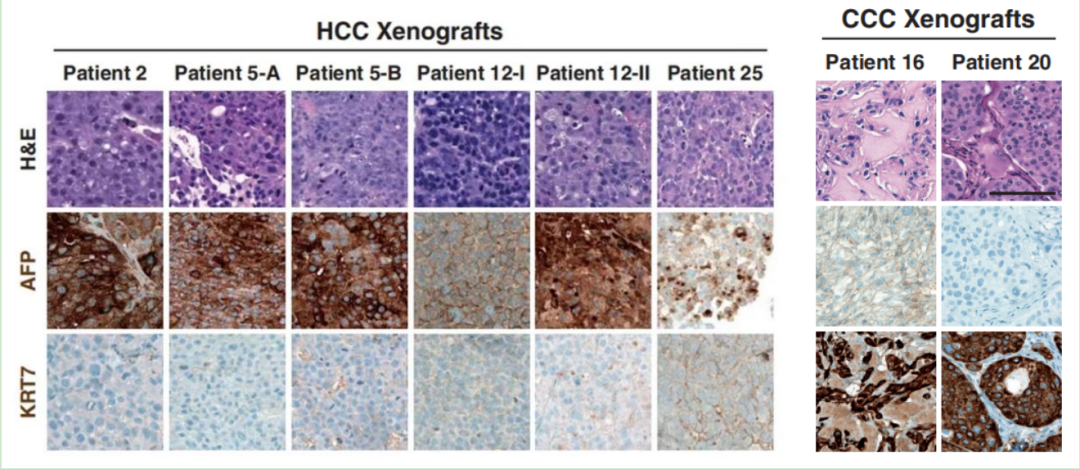
图4 HCC和CCC类器官的异种移植瘤HE染色图和生物标志物IHC图
二
成功生成CCC类器官且还原亲代肿瘤特征
在原发性肝癌的患者中,有4例肝内胆管癌和1例罕见的肝内胆管癌-淋巴上皮瘤样胆管癌。形态学上,CCC类器官形成类似于HCC类器官致密的球体(图5)。CCC类器官显示出与亲代肿瘤相同的特征,并与原代肿瘤活检中一致,表达典型胆道标志物KRT7和KRT19(图6)。证明CCC类器官与亲代肿瘤特征有较高的一致性。
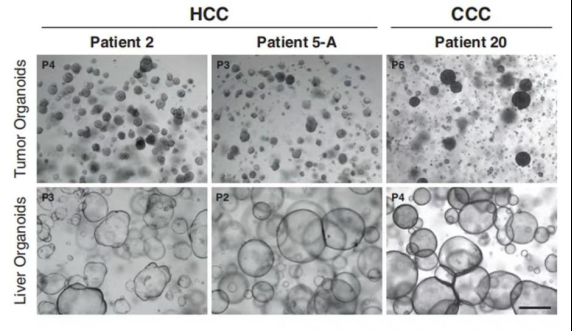
图5 不同患者成对肿瘤和正常肝组织类器官明场图
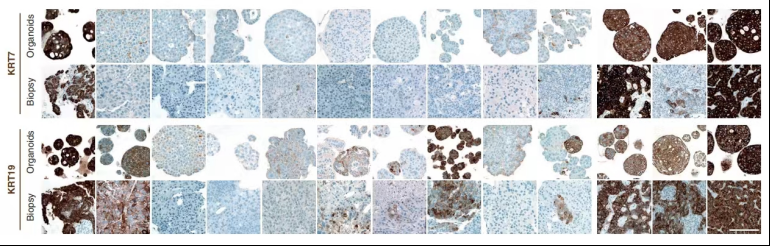
图6 类器官和活检组织胆道标志物IHC图
三
HCC类器官和CCC类器官对索拉非尼的敏感度不同
用不同浓度的索拉非尼处理HCC类器官后,采用Glo检测细胞活力。体外实验结果显示,索拉非尼呈剂量依赖性抑制HCC类器官生长(图7)。同时,测试了三种 CCC 类器官对索拉非尼的敏感度,其中一种罕见亚型CCC类器官(淋巴上皮瘤样CCC,Patient 16))对索拉非尼敏感,其 IC50值与HCC 类器官对索拉非尼的敏感度相当。
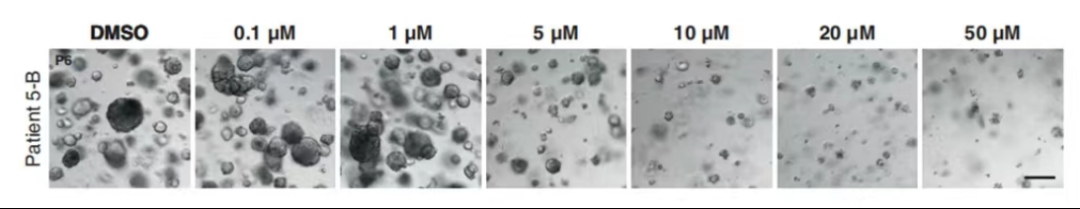
图7 不同浓度索拉非尼处理HCC类器官明场图
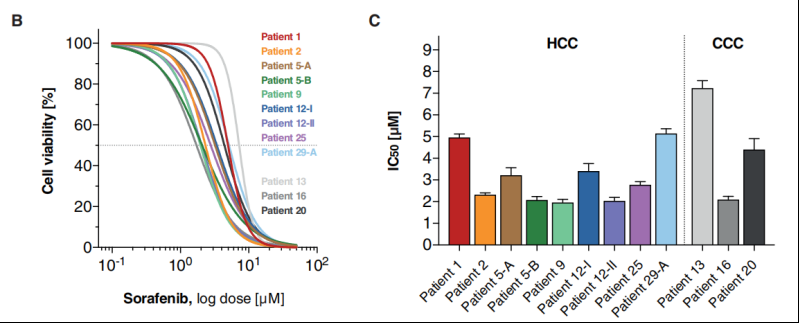
图8 不同浓度索拉非尼处理下细胞活性曲线图; 不同患者来源的HCC和CCC类器官对索拉非尼的IC50值
精科类器官亮点
精科医学作为国内类器官技术转化先行者,对肝癌类器官的相关研究与临床应用更是走在行业前列。我们在肝癌类器官(原位以及转移灶)培养方面积累了丰富经验,且拥有成熟的癌组织超微量建模技术,一份微量样本可以同时实现类器官建模和NGS测序,能够在少量样本的情况下为患者提供更多检测服务,给临床患者带来更大获益。此外,我们还和多家医院和科研机构开展科研和临床合作。目前我们已经在类器官微量建模、类器官鉴定、药物敏感性检测方法、类器官共培养等多个重要技术上实现突破,并已建立相关实验室标准。