08
2022-12
Citation
引文
乳腺癌是女性最常见的恶性肿瘤,发病率也居于女性恶性肿瘤之首。乳腺癌亚型超过20种,由于肿瘤异质性,不同患者在组织学、遗传学、临床表征等方面又各有不同。因此,寻找合适的能够真实反映患者肿瘤异质性的模型严重关系到实验成果向临床应用的转化。
在传统的临床前模型中:细胞系模型操作简便,成本低,但其类型过于单一,且不具有3D结构;人源异种移植模型作为目前肿瘤研究的金标准,虽然能够较为准确概括亲本肿瘤特征,但成本高昂、建模周期长且无法高通量使用。相较二者:类器官在具有高拟合度、短培养周期等优点的同时具备高通量使用的条件,为解决乳腺癌建模问题带来了可能。
类器官与现有模型综合性能对比
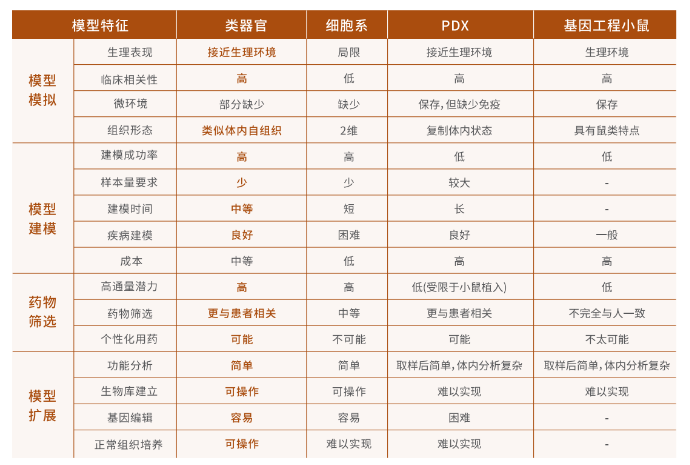
如何建立乳腺癌类器官?
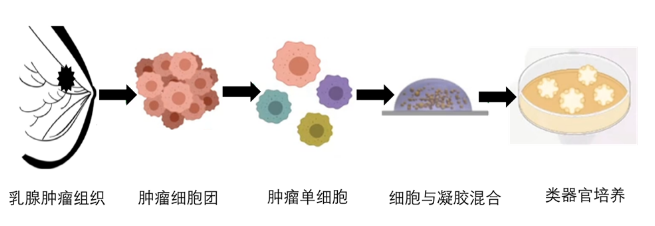
图1 患者来源乳腺癌类器官构建方法
1
“低毒广谱高效”的白藜芦醇
——乳癌类器官助力新药发现
晚期乳腺癌患者,尤其是多药耐药乳腺癌患者迫切需要有效低毒的抗肿瘤药物。
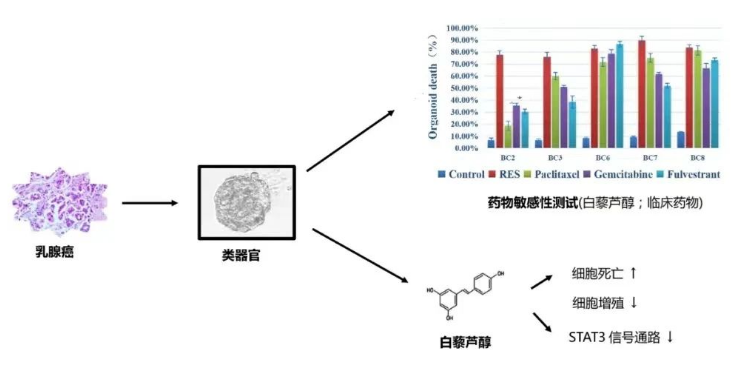
白藜芦醇(RES)是一种广泛存在于葡萄、花生等食物中的天然多酚类化合物。RES在前期临床试验中被证明有预防乳腺癌的潜力,对乳腺癌细胞系有抑制作用。为了进一步验证RES对晚期乳腺癌患者的有效性和普遍性,精科医学首席科学家李宏教授带领团队开展一项白藜芦醇在晚期乳腺癌类器官中的疗效对比验证研究,成功证明了白藜芦醇对晚期乳腺癌类器官有很好的抑制效果。
白藜芦醇原被应用于治疗胰腺癌、直肠癌、急性淋巴细胞白血病等疾病,如今被证明在乳腺癌治疗的潜力。这一成果无疑会为乳腺癌治疗药物开发带来新突破。
2
“铁死亡”研究带来治疗新策略!
——乳癌类器官助力机制探索
“铁死亡”是近年新发现的一种细胞死亡形式,近年来,在肿瘤生物学研究和临床治疗中被广泛关注。
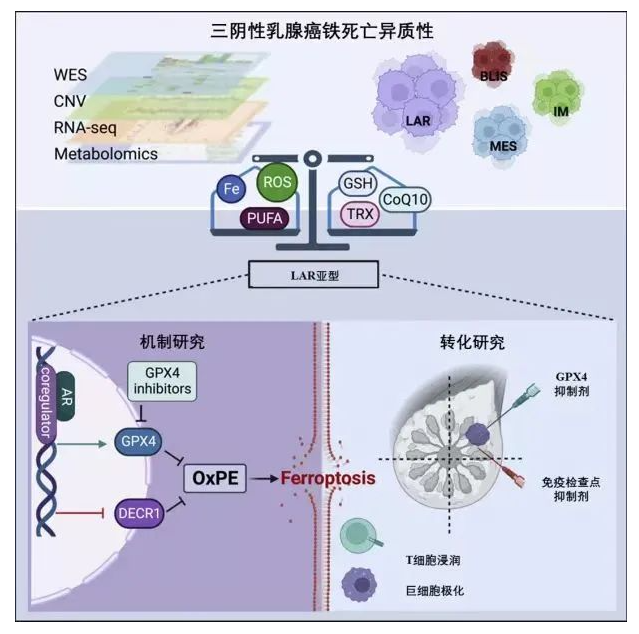
今年10月,邵志敏、江一舟教授团队最新发布的一项研究显示,“铁死亡”在复旦分型亚型之一腔面雄激素受体型(LAR)中更加活跃,且以“谷胱甘肽过氧化物酶4”(GPX4)为核心的谷胱甘肽代谢在LAR型三阴性乳腺癌“铁死亡”调控中有重要地位。基于此结论,团队提出GPX4抑制剂联合免疫治疗或成为LAR型三阴性乳腺癌的新治疗策略。
近几年,类器官已凭借较高的创新性成为疾病研究的瞩目模型,深受基金项目申请和高分杂志的青睐。本文团队借助了患者来源的乳腺癌类器官进一步证明了LAR肿瘤细胞对GPX4抑制剂具有更高的敏感性,也体现出对于类器官技术的高度认可。
3
“试药替身”!
——乳癌类器官助力精准医疗
古有忠臣舍命“为君试药”的美谈,而如今随着科技发展,类器官药敏技术的发展让“试药”不再成为“君主”独享的特权——患者来源的肿瘤类器官将作为患者的“试药替身”反映患者对药物敏感性。
*案例1:
患者王女士,于7年前经医院诊断为浸润性乳腺癌,经6个疗程的新辅助化疗(第1轮用药)进行手术。后持续性药物治疗(第2轮用药方案)。2017年复查,PET-CT显示肝转移,医生开始第4轮用药治疗,达到PR效果。2020年,王女士病情又有进展,MRI显示患者出现骨盆等多发转移瘤,换药后(第5轮用药)患者出现严重副反应,停药。2020年7月,对转移病灶进行穿刺。在患者知情前提下行类器官培养和药物敏感性检测。药敏检测显示:6种治疗方案中,DS8201药效最佳。医生与患者家属沟通后尝试使用DS8201治疗,同时使用地舒单抗对骨转移病灶进行控制,患者在后续随访中疗效达到PR效果。
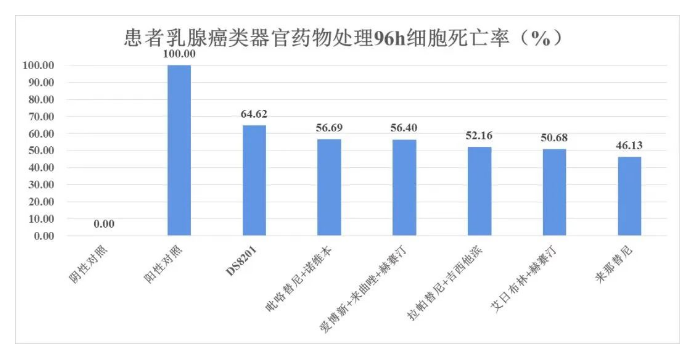
图2 患者乳腺癌类器官药物处理96H细胞死亡率图
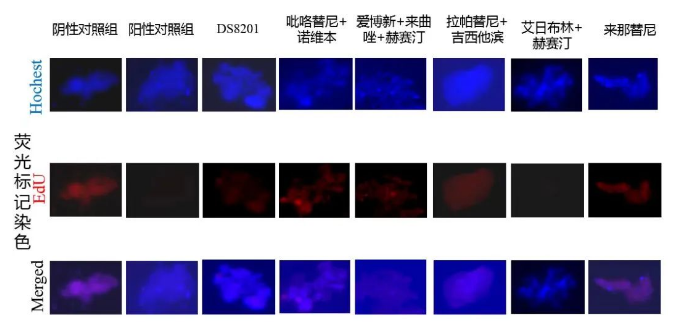
图3 患者乳腺癌类器官药物处理96H荧光标记染色图
*案例2:
患者陈女士(化名)之前确诊为三阴性乳腺癌,在新辅助化疗(表阿霉素、环磷酰胺、多西他赛和卡铂)后肿瘤发生进展。随后接受改良根治性肿瘤切除术和辅助放射治疗。治疗6个月后,她出现了多发肺转移并对卡培他滨表现出耐药性。通过肺转移活检肿瘤样本培养的类器官进行药筛,结果表明:依维莫司、米托蒽醌和长春瑞滨是该患者的潜在候选药物。结合类器官药敏试验和临床实践指南,改用依维莫司和长春瑞滨用药治疗3个月后,患者病情稳定。
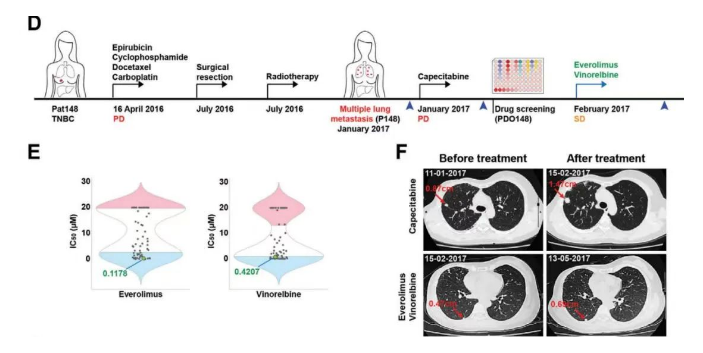
图4 类器官药筛与患者的治疗过程与反应
近几十年来,人们对乳腺癌发生的认识有了很大的提升,治疗手段也取得了很大的进展,但乳腺癌治疗,尤其是晚期乳腺癌以及三阴性乳腺癌的用药仍然是一个难题。经历多线用药后的乳腺癌患者往往表现出多药耐药性,类器官药敏技术“替身试药”能更好地为患者量身定制最适合的用药方案,是精准医疗时代制定患者个体化治疗方案的好帮手。
精科亮点
