19
2023-01
精科
医学
News
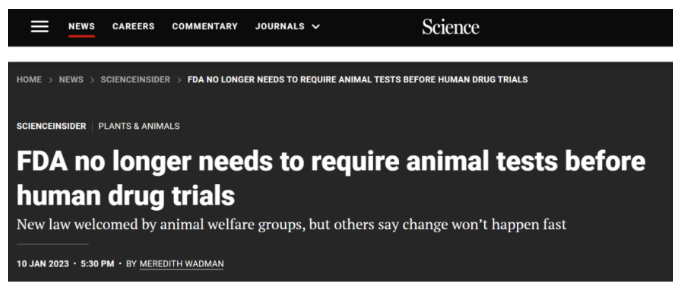
2023年来临之际,美国总统Joe Biden签署了新法案——新的药物临床试验申请无需在动物身上进行测试即可获得美国食品和药品管理局(FDA)的批准。这一重大变革也于今年1月10日在Science期刊上占领了醒目版面,并迅速在学术界引发广泛讨论。

事实上,这已不是美国官方第一次尝试对动物临床试验相关法案进行修改。去年9月,美国参议院通过美国食品药品监督管理局现代化法案(FDA Modernization Act 2.0),取消了之前对动物临床试验的严格要求,并建议在适当的时候使用替代方法。
1
渊源与困局
“动物试验强制令”设立于1938年,起因是多起严重的药品安全事故。为了避免悲剧重演,1938年《联邦食品、药品和化妆品法案》(FDCA)规定所有药物上市前都需要提供安全性证据。药物被正式应用于人体之前必须先在动物身上测试安全性也成了过去几十年唯一的选择。
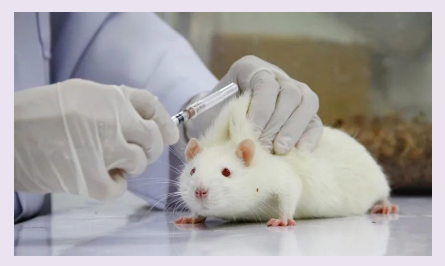
然而,随着动物试验的普及与推广,新的问题应运而生。自2008起,美国每年使用的实验猴数量多达7万,数以千万的实验鼠被用于临床毒理试验……实验动物的大量使用除了引起动物保护组织人士的反对,还使许多公司饱受困扰——动物模型价格涨势迅猛导致研发成本水涨船高。此外,尽管药企每年使用数以万计的动物进行毒性测试,仍会有90%的药物进入临床后会出现不安全或无效,著名案例包括曾在全球造成上万例“海豹儿”悲剧的沙利度胺药(点击查看详情“反应停事件”)。
正是多种因素的综合,为动物强制实验强制令取消埋下了伏笔。法案的主要推动者、人道经济中心研究和监管政策主任Tamara Drake表示,法案的正式取消不仅是一场巨大的变革,也是行业与需治疗患者的一场双赢。他认为:在批准药物进行人体试验时,FDA应更多地依靠计算机建模、“器官芯片”和其他在过去10至15年开发的非动物方法。
寻求立法取缔动物实验之路,美国并非独行者。2013年欧盟已经全面禁止化妆品动物试验。除却道德因素,人们希望将新药更加高效推向市场。大量药物在临床试验中验证失败的根本原因就是传统的临床前模型无法准确预测人体的用药效果。约翰·霍普金斯大学研究动物试验替代品的科学家兼律师Paul Locke表示,虽然有很多药物是通过动物实验开发出来的,但当遇到一些更难治的疾病——比如神经系统疾病和肿瘤时,动物模型表现其实欠佳,“我们需要新的技术来真正了解这些疾病的分子机制,我认为替代方案很有希望”。
2
类器官模型或成首选替代模型
法案的发布使逐步取缔动物试验的趋势渐渐明晰,然而风口当下,哪种“替代方案”能突出重围,成为药物研发人员的首选呢?
实际上国自然基金“十四五”发展规划就为我们画好了重点——文件中提到未来我国将在多个方向明确支持类器官技术发展与医药应用场景的大力开拓,给足了类器官领域先行者们继续前行的信心!

内容来自国家自然基金会“十四五”规划正文
3
类器官是什么?
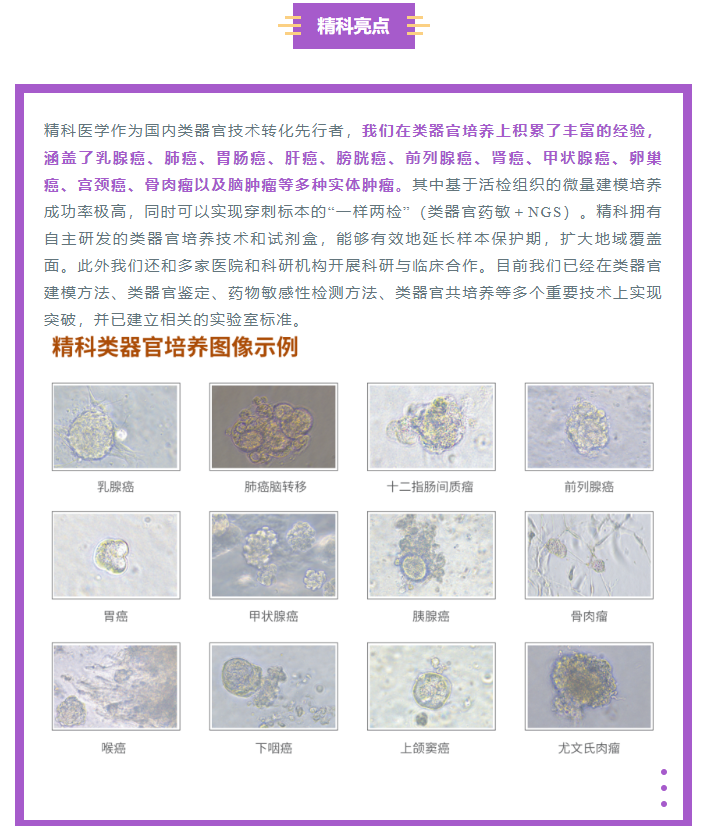
类器官是利用干细胞或患者组织在3D培养条件下形成的多细胞立体结构,在结构以及功能上高度模拟人体器官和病变组织(如癌症),能够形成器官类似的空间结构并且分化出对应功能,具备增殖分化、自我组装、长期培养、遗传稳定等特点。
作为优秀的体外3D模型,类器官在精准医学、疾病模型、药物研发、毒理学、再生医学等多个方面都具有广泛的应用前景。值得一提的是在医药研发过程中,类器官突破了目前临床前模型如2D细胞系、实验动物的局限,真正实现了药物在临床前与患者组织的接触和精准药效评价。
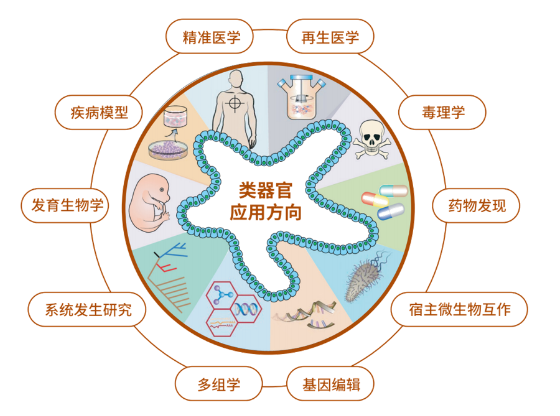
近年来各界在减少不必要的动物试验上的努力,同时推动了人源体系高仿生、高通量的如类器官芯片、类器官等创新模型的发展。FDA这一新政的推出,无疑提示着未来风向。而作为与之紧密联系的生物医药领域从业者,各大医疗科研机构、高校以及企业也应关注动物试验被逐步取缔的这一趋势,及时布局,迎接挑战,把握发展先机!